乙烯
【乙烯的结构】
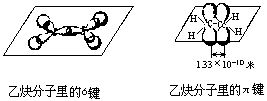
实验表明,乙烯分子里的C=C双键的键长是1.33×10-10米,乙烯分子里的2个碳原子和4个氢原子都处在同一个平面上。它们彼此之间的键角约为120°。乙烯双键的键能是615千焦/摩,实验测得乙烷C—C单键的键长是1.54×10-10米,键能348千焦/摩。这表明C=C双键的键能并不是C—C单键键能的两倍,而是比两倍略少。因此,只需要较少的能量,就能使双键里的一个键断裂。这是乙烯的性质活泼,容易发生加成反应等的原因。
在形成乙烯分子的过程中,每个碳原子以1个2s轨道和2个2p轨道杂化形成3个等同的sp2杂化轨道而成键。这3个sp2杂化轨道在同一平面里,互成120°夹角。因此,在乙烯分子里形成5个σ键,其中4个是C—H键(sp2—s)1个是C—C键(sp2—sp2);两个碳原子剩下未参加杂化的2个平行的p轨道在侧面发生重叠,形成另一种化学键:π键,并和σ键所在的平面垂直。如:乙烯分子里的C=C双键是由一个σ键和一个π键形成的。这两种键的轨道重叠程度是不同的。π键是由p轨道从侧面重叠形成的,重叠程度比σ键从正面重叠要小,所以π键不如σ键牢固,比较容易断裂,断裂时需要的能量也较少。
【乙烯的物理性质】
乙烯在常温常压下为无色气体,稍有香甜气味,比空气稍轻,难溶于水。沸点(常压)-103.71℃,熔点—169.15℃。
【乙烯的化学性质】
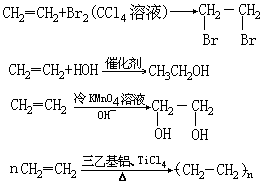
乙烯可燃,燃烧时火焰明亮。与空气形成爆炸性混合物。爆炸极限:下限3~3.5%,上限16~29%。由于乙烯分子中存在双键,性质活泼,容易进行加成反应。氧化反应和加聚反应。如:
【乙烯的实验室制法】
实验室一般是在加热条件下,用浓硫酸使乙醇脱水制取。其中浓硫酸起脱水剂和催化剂作用。在约140℃时,乙醇脱水生成乙醚(C2H5)2O;在约170℃时,生成乙烯。
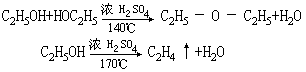
这是在有机化学反应中,反应物相同,反应条件不同而生成物不同的典型例之一。实验装置如图。检查装置气密性后,先在烧瓶中加入10毫升乙醇,然后分批缓缓加入浓硫酸共约30毫升。在乙醇中加入浓硫酸时,由于发生化学作用而放大量热,要冷却后再继续加浓硫酸,防止乙醇大量气化。再向烧瓶里加入几片碎瓷片。为了控制混合液受热温度在170℃左右,须把温度计的水银球浸入混合液中。加热时,要使混合液的温度迅速越过140℃温度区,这样,可以减少副产物乙醚的生成。混合液的温度达到170℃时,即有乙烯产生。在加热过程中,混合液的颜色会逐渐变棕色以至棕黑色。这是由于乙醇部分发生碳化的结果。在170℃时,生成的气体并非纯净的乙烯,其中常杂有少量SO2。由于在加热条件下,浓硫酸除使乙醇发生脱水反应外,还会使乙醇(或其它生成物)发生氧化反应,浓硫酸还原产生SO2。要获得较纯净的乙烯,可以把由烧瓶出来的气体先经10%NaOH溶液洗气,然后再收集。乙烯难熔于水,应该用排水法收集。收满乙烯的集气瓶,盖好毛玻璃片后倒放在实验桌上。停止加热时,要先把导管从水槽里撤出,防止因烧瓶冷却使水倒吸。实验后,应待烧瓶里的残粥状黑色混合物以及温度计冷却后再清洗。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
