溶度积
【定义】 在一定温度下,难溶电解质在它的饱和溶液中达成溶解平衡时,离子浓度(严格说应为离子活度)的幂乘积,叫溶度积,习惯上用Ksp表示。例如
MmNn(固体)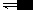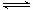 mMn++nNm- ,
mMn++nNm- ,
则有
Ksp==[Mn+]m[Nm-]n。
溶度积数值的大小表示电解质在溶剂中的溶解能力。
【说明】
1. 在一定温度下,一种物质的Ksp是常数。例如在25℃,Ksp(AgCl) =1. 56 X 10-10 ,Ksp(CaC03) =8. 7 X 10-9。
2.难溶电解质在溶剂中,当溶解和沉淀的速率相等时,便在固体和溶液中离子间达成动态平衡,这时的溶液是饱和溶液。根据平衡移动原理,可以得到
(1)当[Mn+]m[Nm-]n>Ksp时,溶液呈过饱和状态,将析出沉淀。
(2)当[Mn+]m[Nm-]n=Ksp时,溶液呈饱和状态,表面上看溶液中既没有沉淀析出,沉淀也不溶解。
(3)当[Mn+]m[Nm-]n<Ksp时,溶液呈不饱和状态,存在于溶液中的沉淀将溶解。这三条规律合起来就叫溶度积原理。它是解决难溶电解质溶解问题的依据。
3.根据溶度积的值可以估计和比较同类难溶电解质的溶解度大小:溶度积越小,表示该物质溶解度越小;还可以判断在一定条件下沉淀的生成和溶解的可能性以及判断体系中有多种离子共存时各种离子生成沉淀的先后次序。附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
