酸
【酸】电解质电离时所生成的阳离子全部是氢离子(H+)的化合物。它能和碱或碱性氧化物反应生成盐和水,能与某些金属反应生成盐和氢气,水溶液有酸味并能使指示剂变色,如紫色石蕊变红。根据酸分子中可被金属原子置换的氢原子数目,可分为一元酸(如HCl)、二元酸(如H2SO4)、多元酸(如H3PO4)等。根据酸在水溶液中产生氢离子程度的大小(即电离度的大小),可分为强酸(如HCl、H2SO4、HNO3、HClO4等)和弱酸(如H2CO3、H2S等)。根据酸根的组成成分又可分为含氧酸(如H2SO4)和无氧酸(如HCl)。此外,根据酸碱的质子理论和电子理论,还有质子酸和路易斯酸等,因而使得“酸”这个概念包括的范围极为广泛,而且又赋予它新的含义。
【说明】
1. H30+(水合氢离子)是H+和H20结合而成的。在书写电离方程式时,为了简便起见,通常仍以H+代替H30+ 。
2. 根据酸在水溶液中电离度的大小,酸分为强酸和弱酸。根据酸分子中可以电离的氢原子个数,酸分为一元酸(如HNO3)、 二元酸(如H2S04)和三元酸(如H3P04)。根据酸中是否含氧,酸分为含氧酸和无氧酸。
3. 无氧酸称氢某酸。如HF叫氢氟酸,H2S叫氢硫酸。在无氧酸中,HC1、HBr和HI是强酸,其余都是弱酸。简单含氧酸 通常叫某酸,如硫酸(H2S04)、碳酸(H2CO3)。某一成酸元素如果能形成多种含氧酸,就按成酸元素的氧化数高低命名,如高氯酸 (HClO4、氯酸(HC103)、亚氯酸(HC102)、次氯酸(HClO)。两个简单含氧酸缩去一分子水而形成的酸,叫做焦酸(或称一缩某酸、重酸),例如,2H2S04 = H2S207(焦硫酸)+H20;2H2Cr04=H2Cr207(重铬酸)+H2O
酸分子中的氢氧塞数等于成酸元素的氧化数,这种酸叫原某酸,如 原磷酸[P(OH)5 即 H5PO5],原硅酸[Si(OH)4,即 H4Si04]。一个正酸分子失去一分子水而形成的酸,叫做偏某酸,如偏磷酸 (HP03)、偏硅酸(H2Si03)。含有过氧键(一0—O—)的酸叫过酸,如过一硫酸(H2SO5),过二硫酸(H2S2O8)。
4. 把含氧酸的化学式写成MOm(OH)n(M是非金属),就 能根据m值判断常见含氧酸的强弱。
m=0,极弱酸,如硼酸(H3B03)。
m=1,弱酸,如亚硫酸(H2S03)。
m=2,强酸,如硫酸(H2S04)、硝酸(HN03)。
m=3,极强酸,如高氯酸(HC104)。
5. 强酸在水溶液中完全电离;弱酸在水溶液中存在电离平衡 HA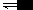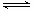 H+ + A-。
H+ + A-。
K=[H+][A-]/[HA]
电离平衡常数K随弱酸的浓度和温度不同,变化不大。
6. 定义2是根据酸碱质子理论对酸下的定义。
A 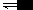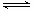 H+ +B
H+ +B
HC1= H++Cl-
H2PO4- 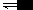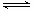 H+ +HPO42-
H+ +HPO42-
NH4+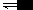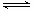 H+ +NH3
H+ +NH3
HC1、H2SO4叫分子酸,H2P04-、NH4+叫离子酸,A和B互为共轭酸碱对。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
